Kemijski sastav stanica
Sadržaj

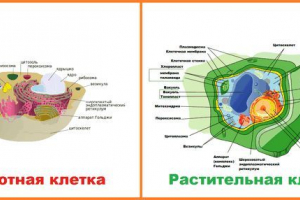
Stanice - Osnovna jedinica života na Zemlji. Ima sve znakove življenja organizma: raste, množi, razmjene s tvarima i energijom za okoliš, reagira na vanjske podražaje. Početak biološke evolucije povezana je s pojavom staničnih oblika života na Zemlji. Unicelularni organizmi su postojeće stanice odvojeno jedan od drugoga. Tijelo svih višestaničnih životinja i biljaka - izgrađena od više ili manje stanica koje su vrste blokova koji čine složeni organizam. Bez obzira na to je li stanica holistički životni sustav - poseban organizam ili je samo dio toga, obdarena je skupom značajki i svojstava zajedničkih za sve stanice.
Kemijski sastav stanica

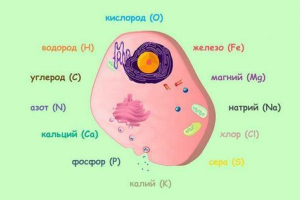
U stanicama su pronađeni oko 60 elemenata periodičnog mendeleev periodičnog, koji se nalazi u neživoj prirodi. To je jedan od dokaza o zajednici življenja i neživog prirode. U živim organizmima najčešći su vodik, kisik, ugljen i dušik, koji čine oko 98% mase stanica. To je zbog posebnosti kemijskih svojstava vodika, kisika, ugljika i dušika, zbog čega su se pokazali da su najprikladniji za formiranje molekula koji obavljaju biološke funkcije. Ova četiri elementa mogu formirati vrlo jake kovalentne veze sparavanjem elektrona koji pripadaju dva atoma. Kovalentno povezani atomi ugljika mogu tvoriti okvire bezbrojnih različitih organskih molekula. Budući da ugljikovi atomi lako tvore kovalentne veze s kisikom, vodikom, dušikom, kao i sa sumporom, organske molekule dosežu iznimnu složenost i razne strukture.
Osim četiri glavna elementa u stanici u vidljivim količinama (10y i 100y Postotak kamata) su sadržani željezo, kalij, natrij, kalcij, magnezij, klor, fosfor i sumpor. Svi ostali elementi (cinkov, bakar, jod, fluor, kobalt, mangan i tako dalje.) su u kavezu u vrlo malim količinama i stoga se nazivaju elementi u tragovima.
Kemijski elementi dio su anorganskih i organskih spojeva. Anorganski spojevi uključuju vodu, mineralne soli, ugljični dioksid, kiselina i bazu. Organske veze su Proteini, nukleinske kiseline, ugljikohidrati, Mast (lipidi) i Lipoidi.
Neki proteini sadrže sumpor. Dio nukleinskih kiselina je fosfor. Hemoglobin molekula uključuje željezo, magnezij sudjeluje u izgradnji molekule klorofil. Mikroelementi, unatoč izuzetno niskom sadržaju u živim organizmima, igraju važnu ulogu u procesima života. Jod Uključeni u hormon štitne žlijezde - tiroksina, kobalt - u sastavu vitamina u12Hormon otočnog dijela gušterače - inzulin - sadrži cinkov. U nekim ribama, mjesto željeza u molekulama pigmenata koji nose kisik zauzima bakar.
Anorganske tvari

Voda
N2O - najčešća veza u živim organizmima. Njegov sadržaj u različitim stanicama fluktuira u prilično širokim granicama: od 10% u caklinu zuba do 98% u tijelu meduze, ali je oko 80% tjelesne težine. Iznimno važnu ulogu vode u osiguravanju procesa života je zbog svojih fizikalno-kemijskih svojstava. Polaritet molekula i sposobnost formiranja vodikovih veza čini vodu s dobrim otapalom za ogromnu količinu tvari. Većina kemijskih reakcija nastaje u stanici se može pojaviti samo u vodenoj otopini. Voda sudjeluje u mnogim kemijskim transformacijama.
Ukupan broj vodikovih veza između molekula vode varira ovisno o t°. S T° Taljenje leda uništava približno 15% vodikovih veza, na t ° 40 ° C - pola. Kada se prebacite na plinovito stanje, sve vodikove veze su uništene. To objašnjava visok specifični toplinski kapacitet vode. S promjenom u t ° vanjskog okruženja, voda apsorbira ili naglašava toplinu zbog prekida ili nove formiranja vodikovih veza. Na taj način fluktuacioni t ° unutar stanica su manji nego u okolišu. Visoka toplina isparavanja ovisi o učinkovitim mehanizmu prijenosa topline u biljkama i životinjama.
Voda kao otapalo sudjeluje u fenomenima osmoze koja ima važnu ulogu u životu tijela stanice. Osmoza se naziva penetracijom molekula otapala kroz polupropusnu membranu u otopinu bilo koje tvari. Polukruže se nazivaju membrane koje preskoči molekule otapala, ali molekule (ili ione) otopljene tvari nedostaju. Prema tome, osmoza je jednostrana difuzija molekula vode u smjeru otopine.
Mineralne soli

Većina anorganskih B-u stanicama je u obliku soli u disocijaciji ili u čvrstom stanju. Koncentraciju kationa i aniona u ćeliju iu okolišu koje ga okružuje. Stanica sadrži dosta i puno na. U izvanstaničnom mediju, na primjer, u krvnoj plazmi, u morskoj vodi, naprotiv, mnogo natrija i malih kalija. Navodnja stanica ovisi o omjeru koncentracija na iona+, K+, Ca2+, Mg2+. U tkivima višestaničnih životinja, K je dio višestanične tvari koja osigurava kvaku stanice i njihovo naručeno mjesto. Osmotski tlak u ćeliji i njezina puferska svojstva ovise o koncentraciji soli. Buffff je sposobnost stanice da održava slabo poznatu reakciju njezina sadržaja na konstantnoj razini. Bifessions unutar ćelije uglavnom daje ione2Ro4 i nra42-. U izvanstaničnim tekućinama iu krvi, uloga međuspremnika igra2TAKO3 i nso3-. Anioni vežu ions H i hidroksid iona (on-), tako da se reakcija unutar stanice ekstracelularnih tekućina praktički ne mijenja. Netopljive mineralne soli (na primjer, fosforni CA) osigurava snagu kosti kralježnjaka i mekušaca.
Stanice organskih stanica
Proteini
Među organskim tvarima, stanice proteina su na prvom mjestu u broju (10 - 12% ukupne mase stanice) i vrijednost. Proteini su polimeri visoki molekularni mase (s molekulskom masom od 6000 do 1 milijun. i iznad) čiji su monomeri aminokiseline. Živi organizmi koriste 20 aminokiselina, iako ima mnogo više. Sastav bilo koje aminokiseline uključuje amino skupinu (-NH2), s osnovnim svojstvima i karboksilnom skupinom (-son) s kiselim svojstvima. Dvije aminokiseline povezane su u jednoj molekuli uspostavljanjem HN-CO komunikacije s otpuštanjem molekule vode. Odnos između amino skupine jedne aminokiseline i karboksila je drugi nazvan peptid. Proteini su polipeptidi koji sadrže desetke i stotine aminokiselina. Molekule različitih proteina se međusobno razlikuju s molekulskom težinom, brojem, sastavom aminokiselina i sekvencom njihovog položaja u polipeptidnom lancu. Jasno je da se proteini razlikuju ogromnom raznolikošću, njihov broj svih vrsta živih organizama procjenjuje se brojem od 10deset - deset12.
Lanac aminokiselinskih jedinica povezanih kovalentnim peptidnim vezama u određenoj sekvenci naziva se primarna struktura proteina. U stanicama, proteini imaju pogled na spiralna upletana vlakna ili loptice (globule). To je zbog činjenice da je u prirodnom proteinu, polipeptidni lanac postavljen strogo na određeni način ovisno o kemijskoj strukturi aminokiselina uključenih u njegov sastav.

U početku se polipeptidni lanac pretvara u spiralu. Postoji atrakcija između atoma susjednih okreta i oblikovanih vodikovih veza, posebno, između NH- i skupina smještenih na susjednim okretama. Aminokiselinski lanac, uvijen u obliku spiralnih oblika sekundarne proteinske strukture. Kao rezultat daljnjeg polaganja spirale, nastaje konfiguracija specifična za svaki protein, naziva se tercijarna struktura. Tercijarna struktura je posljedica djelovanja sila kvačila između hidrofobnih radikala dostupnih u nekim aminokiselinama i kovalentnim vezama između cistein amino kiselina SH grupa (S-S-S-komunikacija). Broj aminokiselina s hidrofobnim radikalima i cisteinom, kao i redoslijedom njihovog položaja u polipeptidnom lancu specifični su za svaki protein. Prema tome, osobitosti tercijarne strukture proteina određuju se primarnom strukturom. Biološka aktivnost proteina pokazuje samo u obliku tercijarne strukture. Stoga zamjena čak jedne aminokiseline u polipeptidnom lancu može dovesti do promjene u konfiguraciji proteina i na smanjenje ili gubitak njegove biološke aktivnosti.
U nekim slučajevima, molekule proteina se međusobno kombiniraju i mogu obavljati svoju funkciju samo u obliku kompleksa. Hemoglobin je kompleks od četiri molekule i samo u takvom obliku može pričvrstiti i transportirati. Takvi agregati su četvrtina struktura proteina. Što se tiče njezina sastava, proteini su podijeljeni u dvije glavne klase - jednostavno i složeno. Jednostavni proteini sastoje se samo od nukleinskih kiselina aminokiselina (nukleotida), lipida (lipoproteina), IU (metaloproteidi), P (fosfopropristi).
Funkcije proteina u stanici su izuzetno raznolike. Jedna od najvažnijih funkcija izgradnje: proteini su uključeni u formiranje svih stanica i stanica stanice, kao i intracelularne strukture. Enzimska (katalitička) uloga proteina je iznimno važna. Enzimi ubrzaju kemijske reakcije koje se pojavljuju u ćeliji, u 10ki i 100n Milijun puta. Funkcija motora osigurava posebni kontraktilni proteini. Ovi proteini su uključeni u sve vrste pokreta na koje su stanice i organizmi sposobni za: treperenje cilije i premlaćivanje okusa od najjednostavnijeg, kratica mišića kod životinja, kretanje lišća u biljkama, itd. Transportna funkcija proteina je pričvrstiti kemijske elemente (na primjer, hemoglobin pridružuje) ili biološki aktivne tvari (hormoni) i prenose ih u tkiva i tijela tijela. Zaštitna funkcija je izražena u obliku razvoja posebnih proteina nazvanih antitijela, kao odgovor na prodiranje u tijelo izvanzemaljskih proteina ili stanica. Antitijela se vežu i neutraliziraju stranim tvarima. Proteini igraju važnu ulogu kao izvori energije. S punim cijepanjem 1g. Proteini se ističu 17,6 k m (~ 4,2 kcal).
Ugljikohidrati

Ugljikohidrati ili saharidi - organske tvari s općom formulom (CH2ON. U većini ugljikohidrata, broj atoma H je veći od broja atoma o, kao u molekulama vode. Stoga su se te tvari nazvali ugljikohidratima. U dnevnom kavezu, ugljikohidrati su u količinama koje ne prelaze 1-2, ponekad 5% (u jetri, u mišićima). Najbogatiji u ugljikohidratima biljnih stanica, gdje njihov sadržaj doseže u nekim slučajevima 90% mase suhe tvari (sjemenke, gomolji krumpira itd.D.).
Ugljikohidrati su jednostavni i složeni. Jednostavni ugljikohidrati se nazivaju monosaharidi. Ovisno o broju ugljikohidrata atoma u molekuli monosaharida, nazivaju se trioses, tetroza, pateose ili heksadeze. Od šest ugljikovih monosaharida - heksoza - glukoza, fruktoza i galaktoza imaju najvažnu važnost. Glukoza je sadržana u krvi (0,1-0,12%). Pentozovi riboza i deoksiriboza dio su nukleinskih kiselina i ATP. Ako se dva monosaharida kombiniraju u jednoj molekuli, takva se veza naziva disaharid. Prehrambeni šećer dobiven od štapova ili šećerne repe sastoji se od jedne molekule glukoze i jedne molekule fruktoze, mlijeka šećera - od glukoze i galaktoze.
Kompleksni ugljikohidrati formirani mnogi monosaharidi nazivaju se polisaharidi. Monomer takvih polisaharida, poput škroba, glikogena, celuloze, glukoza. Ugljikohidrati obavljaju dvije glavne funkcije: izgradnju i energiju. Celuloza tvori zidove biljnih stanica. Sofisticirani polisaharid Chitin služi kao glavna strukturna komponenta vanjskog kostura od artropoda. Funkcija izgradnje chitin izvodi gljive. Ugljikohidrati igraju ulogu glavnog izvora energije u ćeliji. U procesu oksidacije 1 g. Ugljikohidrati su izdali 17,6 KJ (~ 4,2 kcal). Škrob u biljkama i glikogen kod životinja se pohranjuju u stanicama i služe kao energetska rezerva.
Nukleinske kiseline

Vrijednost nukleinskih kiselina u ćeliji je vrlo velika. Značajke njihove kemijske strukture pružaju mogućnost skladištenja, prijenosa i prijenosa baštinom od strane dječjih stanica informacija o strukturi proteinskih molekula, koje se sintetiziraju u svakom tkivu u određenoj fazi individualnog razvoja. Budući da je većina nekretnina i znakova stanica posljedica proteina, jasno je da je stabilnost nukleinskih kiselina najvažnija uvjet za normalan život stanica i cijelih organizama. Bilo kakve promjene u strukturi stanica ili aktivnost fizioloških procesa u njima, koje utječu na vitalnu aktivnost. Proučavanje strukture nukleinskih kiselina je iznimno važna za razumijevanje nasljeđivanja karakteristika organizma i obrazaca funkcioniranja, obje pojedine stanice i stanične sustave - tkiva i organa.
Postoje 2 vrste nukleinskih kiselina - DNA i RNA. DNA - polimer koji se sastoji od dvije nukleotidne spirale, zatvorenike tako da se formira dvostruka spiralna. Molekule monomera su nukleotidi koji se sastoje od base dušika (adenin, timin, gvanin ili citozin), ugljikohidrat (dezoksiriboza) i ostataka fosforne kiseline. Azotyst Baze u molekuli DNA međusobno su međusobno povezani s različitim brojem N-linkova i nalaze se u parovima: Adenin (a) je uvijek protiv timina (T), gvanina (d) protiv citozina (c).
Nukleotidi su međusobno spojene ne slučajno, ali selektivno. Sposobnost da se potaknuto adeniranje s vime i gvaninom s citozinom naziva se komplementarna. Komplementarna interakcija određenih nukleotida objašnjava se osobitošću prostornog rasporeda atoma u njihovim molekulama koje im omogućuju zatvaranje i formiranje N-veza. U polinukleotidnom lancu, susjedni nukleotidi su međusobno povezani kroz šećer (dezoksiriboza) i ostatak fosforne kiseline. RNA, kao i DNA je polimer čiji su monomeri nukleotidi. Dušične baze triju nukleotida su jednake kao dio DNA (A, G, C) - četvrti uracil (Y) prisutan je u RNA molekuli umjesto vremena. RNA nukleotidi se razlikuju od DNA nukleotida i na strukturi ugljikohidrata uključenog u njihov sastav (riboza umjesto disoksiriboze).
U lancu RNA nukleotida se kombiniraju formiranjem kovalentnih veza između riboze jednog nukleotida i ostatka fosforne kiseline drugog. Struktura se razlikuje od dvije lančane RNA. Dva lančana RNA su čuvari genetskih informacija u brojnim virusima, t.E. Obavljaju funkcije kromosoma. Jedna lančana RNA prijenos informacija o strukturi proteina od kromosoma do mjesta njihove sinteze i sudjeluje u sintezi proteina.
Postoji nekoliko vrsta jednog lanca RNA. Njihova imena su zbog funkcije ili mjesta u stanici. Većina citoplazme RNA (do 80-90%) je ribosomalna RNA (RRNA) sadržana u ribosomima. Molekule RRNA su relativno male i sastoje se u prosjeku 10 nukleotida. Druga vrsta RNA (IRNN) koja nosi informacije o sekvenci aminokiselina u proteinima koji se sintetiziraju do ribosoma. Veličina ove RNA ovisi o duljini dijela DNA na kojoj su sintetizirani. Prijevoz RNA obavlja nekoliko funkcija. Oni dostavljaju aminokiseline na mjestu sinteze proteina, "prepoznaju" (na principu komplementarnosti) tripleta i RNA koja odgovara prijenosnoj aminokiselini provodi točnu orijentaciju aminokiseline na ribosomu.
Masti i lipidi

Masti su spojevi masnih visokih molekularnih težina i trukatomijskog alkohola glicerina. Masti se ne otapaju u vodi - oni su hidrofobni. Uvijek postoje druge kompleksne hidrofobne tvari u kavezu, nazvane lipoidi.Jedna od glavnih funkcija masti je energija. Tijekom cijepanja 1 g. Masti do S2 i N2O velikoj količini energije je oslobođena - 38,9 k m (~ 9,3 kcal). Sadržaj masti u staniku u rasponu od 5-15% mase suhe tvari. U stanicama živahnog tkiva, količina masti se povećava na 90%. Glavna funkcija masti u životinji (i djelomično - povrća).
S punom oksidacijom od 1 g masti (u ugljični dioksid i vodu), razlikuje se oko 9 kcal energije. (1 kcal = 1000 calcalo (CAL, CAL) - incident jedinica količine radova i energije jednaka količini topline potrebne za grijanje 1 ml vode na 1 ° C sa standardnim atmosferskim tlakom od 101,325 kPa-1 kcal = 4,19 Kj). Kada se oksidiraju (u tijelu), 1 g proteina ili ugljikohidrata se dodjeljuje samo oko 4 kcal / g. Na različitim vodenim organizmima - od neenicalularnih diatoma algi do divovskih morskih pasa - masnoće traži "plovak", smanjujući prosječnu gustoću tijela. Gustoća životinjske masti je oko 0,91-0,95 g / cm³. Gustoća kostiju kralježnice blizu 1,7-1.8 g / cm³, a prosječna gustoća većine drugih tkiva je blizu 1 g / cm³. Jasno je da masnoća treba dosta za "ravnotežu" teški kostur.
Masti i lipidi izvode funkciju izgradnje: oni su dio staničnih membrana. Zbog loše toplinske vodljivosti je sposoban zaštititi funkciju. U nekim životinjama (brtve, kitovi), odgođen je u potkožnom masnom tkivu, formirajući sloj s debljinom do 1 m. Formiranje neki lipoida prethodi sintezi brojnih hormona. Stoga su ove tvari svojstvene funkcijom reguliranja metaboličkih procesa.